K E M I J A - Gimnazija Karlovac
četvrtak, 20.08.2009.
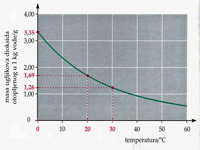
3.31. Topljivost ugljikova dioksida u vodi pri različitim temperaturama
i normalnom atmosferskom tlaku predočena je dijagramom.
Iz svake točke na krivulji u tom dijagramu možemo očitati masu ugljikova dioksida u gramima koji se može otopiti pri određenoj temperaturi u jednom kilogramu vode.Koristi se tim podacima pri rješavanju ovih zadataka.
a) Kako se mijenja topljivost ugljikova dioksida u vodi porastom temperature otopine ?
b) Koliko se grama ugljikova dioksida može najviše otopiti u jednom kilogramu vode pri temperaturi od:
1. 0°C
2. 20°C
3. 30°C
c) Je li otopina koja pri 20°C sadrži jedan gram otopljenog ugljikovog dioksida u
jednom kilogramu vode zasićena ili nezasićena ?
3.32. U 2 kilograma vode otopili smo 2,9 grama ugljikova dioksida i tim smo postupkom priredili zasićenu otopinu pri temperaturi od 25°C.
a) Iskaži masu otapala i masu dobivene u gramima.
b) Iskaži topljivost ugljikova dioksida u vodi pri 25°C masenim udjelom.
c) Predloži postupak kojim bismo smanjili maseni udio otopljenog ugljikova dioksida u zadanoj otopini.
4.14. Gustoća suhog zraka pri 20°C i normalnom atmosferskom tlaku
iznosi 1,205g/L.
a) Izračunaj masu zraka pri navedenim uvjetima kojim je ispunjena
prazna prostorija volumena:
1. 30 kubičnih metara
2. 52 kubična metra
6.12. Napiši znakove kojima označujemo:
a) jedan atom aluminija
b) četiri atoma sumpora
c) tri atoma berilija
6.19. Atomi A,B,C,D,E,F sastoje seod ovih subatomskih čestica:
A: 11p,12n,11e D:16p,18n,16e
B: 16p,16n i 16e E: 13p,14n,13e
C: 3p,4n,3 e F:10p 12n 10e
a) Koji od tih atoma pripadaju istom kemijskom elementu?
b) Napiši naziv i simbol tog elementa.
c) Kako se nazivaju različiti atomi tog elementa?
6.21. Atomi 14N i 15N imaju različiti broj (odaberi točnu tvrdnju):
a) elektrona
b) protona
c) neutrona
d) svih subatomskih čestica
6.24. Odredi broj elektrona, protona i neutrona od kojih se sastoje ovi atomi:
a) 188O
b) 136C
c) 168O
6.42. Napiši znakove za:
a) dva atoma broma
b) tri molekule dušika
c) dvije molekule metana
d) per molekula amonijaka
6.46. Odredi broj i vrstu atoma u slijedećim skupovima molekula:
a) 4F2
b) 10Br2
c) 6 HBr
d) 2NH3
e) 4CH4
6.51. Dopuni rečenice kojima opisujemo građu natrijevog jodida.
1. Natrijev jodid građen je od kationa ……………….. i aniona ……………….
2. Ti ioni izgrađuju …………………… natrijevog jodida.
3. Kristali natrijevog jodida su elektički …………………. .
6.52. Dopuni jednadžbu i odgovori na pitanje.
a) Fe ’ Fe3+ + …………..e-
Koliko protona i elektrona ima atom željeza, a koliko željezov (III) ion ?
6.64. Napiši kemijske formule spojeva: magnezijev sulfid, silicijev dioksid,
aluminijev klorid, natrijev oksid, željezov (III) sulfid, bakrov (I) klorid, cinkov oksid;
6.69. Odredi valenciju atoma u spojevima:
a) NH3, NO2, SO3,CuO, N2O3,Cu2O, H2O
6.77. Pokusom je priređen bezbojni plin P.Taj je plin građen od molekula koje se sastoje od
tri atoma elementa E. Eksperimentalno određena relativna molekulska masa plina P
iznosi 48,0.
a) Izračunaj relativnu atomsku masu elementa E i na osnovi toga identificiraj element E.
b) Napiši kemijsku formulu i naziv plina P.
7.11. Napiši kemijske reakcije označavajući kvantitativno i kvalitativno značenje:
a) Aluminij + kisik ’ aluminijev oksid
b) Elektrolizom taline kalcijevog klorida dobivaju se kalcij i klor
c) Gorenjem željeza u čistom kisiku nastaje željezov(III) oksid
d) Reakcijom cinka i klora nastaje cinkov klorid
e) Reakcijom žive i kisika nastaje živin (II) oksid
7.22. Dopuni jednadžbe ovih kemijskih reakcija:
a) H2 + Br2 ’ ……. HBr
b) ……….HgO’……..Hg + O2
c) ………Fe + …….S ’ Fe2S3
d) CH4 ’ C + …….H2
e) ……..Al + ……..Cl2 ’……… AlCl3
f) ……….Na + O2 ’………Na2O
g) ………H2O ’…..H2 +O2
h) ……….K+ S ’K2S
8.50. Napiši nazive slijedećih soli i kiselina: natrijev sulfat, kalcijev sulfit, bakrov (II) klorid,
magnezijev karbonat, željezov(II) nitrat, sumporna kiselina, sumporasta kiselina,
klorovodična kiselina, ugljična kiselina, dušična kiselina.
Pripremila i objavila:
Anita Grabovac

| < | kolovoz, 2009 | |||||
| P | U | S | Č | P | S | N |
| 1 | 2 | |||||
| 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 17 | 18 | 19 | 20 | 21 | 22 | 23 |
| 24 | 25 | 26 | 27 | 28 | 29 | 30 |
| 31 | ||||||
Kolovoz 2009 (6)
Srpanj 2009 (2)
Dnevnik.hr
Gol.hr
Zadovoljna.hr
Novaplus.hr
NovaTV.hr
DomaTV.hr
Mojamini.tv
Opis bloga
Novosti iz kemije, radni listići, testovi, prezentacije, predavanja, seminari i dr. zanimljivosti vezane uz kemiju i njeno istrazivanje
Linkovi
Dnevnik.hr
Video news portal Nove TV
Blog.hr
Blog servis
drugiE.hr
2.E Gimnazija Klc
Forum.hr
Monitor.hr
Zanimljivosti
 Smjese tvari u kojima su čestice jedne tvari dispergirane (raspršene, raspodijeljene) u drugoj tvari zovemo disperzni sustavi. Disperzni sustavi mogu biti u bilo kojem agregatnom stanju. Na temelju veličine čestica dispergirane tvari, disperzne sustave dijelimo na suspenzije, koloidne sustave ili koloide i prave otopine. Nastavnici u školama vole inzistirati na definicijama tipa 'Koloidni sustavi su disperzni sustavi s veličinama čestica od ... do ...', no ja mislim da to nije bit stvari. Bitno je znati ovo: Suspenzije su disperzni sustavi s najgrubljim (najvećim) česticama. Te čestice predstavljaju zasebnu fazu. Čvrstu tvar iz tekućih suspenzija možemo odijeliti filtracijom ili taloženjem. Primjer suspenzije je suspenzija kakaa ili smrvljene krede u vodi. Koloidni sustavi su disperzni sustavi s nešto manjim česticama. Čvrstu tvar iz tekuće koloidne otopine ne možemo odijeliti filtracijom. U koloidnim sustavima čestice su još uvijek dovoljno velike da se mogu smatrati zasebnom fazom, ali se kinetički ponašaju kao molekule. Koloidne sustave možemo podijeliti prema agregatnom stanju dispergirane tvari i disperznog sredstva. U koloidne sustave spadaju pjena (plinovito u tekućem, npr. pjena za brijanje), čvrsta pjena (plinovito u čvrstom, npr. plovućac, stvrdnuta pur-pjena, stiropor), aerosol (tekuće u plinovitom, npr. sprej, magla, ili čvrsto u plinovitom, npr. dim), emulzija (tekuće u tekućem, npr. majoneza), gel (tekuće u čvrstom, npr. puding, gel za kosu), sol (čvrsto u tekućem, npr. tempera, korekturni lak), i čvrsti sol (čvrsto u čvrstom, npr. rubin, opal). Postoje i drugačije podjele, pa tako neki aerosole dijele na čvrste i tekuće aerosole, što je po mom mišljenju pogrešno jer je aerosol u svakom slučaju plinovit. Koloidni sustavi pokazuju Tyndallov učinak, Brownovo gibanje, adsorpciju, neke zanimljive elektrokemijske pojave i mnoga druga svojstva o kojima bi se moglo još puno napisati. Detalji se mogu naći npr. u Tehničkoj enciklopediji ili na internetu pod ključnim riječima dispersing, dispersed, colloid, foam, gel, sol, aerosol, emulsion, Tyndall effect, Brownian motion, colloid chemistry itd.
Smjese tvari u kojima su čestice jedne tvari dispergirane (raspršene, raspodijeljene) u drugoj tvari zovemo disperzni sustavi. Disperzni sustavi mogu biti u bilo kojem agregatnom stanju. Na temelju veličine čestica dispergirane tvari, disperzne sustave dijelimo na suspenzije, koloidne sustave ili koloide i prave otopine. Nastavnici u školama vole inzistirati na definicijama tipa 'Koloidni sustavi su disperzni sustavi s veličinama čestica od ... do ...', no ja mislim da to nije bit stvari. Bitno je znati ovo: Suspenzije su disperzni sustavi s najgrubljim (najvećim) česticama. Te čestice predstavljaju zasebnu fazu. Čvrstu tvar iz tekućih suspenzija možemo odijeliti filtracijom ili taloženjem. Primjer suspenzije je suspenzija kakaa ili smrvljene krede u vodi. Koloidni sustavi su disperzni sustavi s nešto manjim česticama. Čvrstu tvar iz tekuće koloidne otopine ne možemo odijeliti filtracijom. U koloidnim sustavima čestice su još uvijek dovoljno velike da se mogu smatrati zasebnom fazom, ali se kinetički ponašaju kao molekule. Koloidne sustave možemo podijeliti prema agregatnom stanju dispergirane tvari i disperznog sredstva. U koloidne sustave spadaju pjena (plinovito u tekućem, npr. pjena za brijanje), čvrsta pjena (plinovito u čvrstom, npr. plovućac, stvrdnuta pur-pjena, stiropor), aerosol (tekuće u plinovitom, npr. sprej, magla, ili čvrsto u plinovitom, npr. dim), emulzija (tekuće u tekućem, npr. majoneza), gel (tekuće u čvrstom, npr. puding, gel za kosu), sol (čvrsto u tekućem, npr. tempera, korekturni lak), i čvrsti sol (čvrsto u čvrstom, npr. rubin, opal). Postoje i drugačije podjele, pa tako neki aerosole dijele na čvrste i tekuće aerosole, što je po mom mišljenju pogrešno jer je aerosol u svakom slučaju plinovit. Koloidni sustavi pokazuju Tyndallov učinak, Brownovo gibanje, adsorpciju, neke zanimljive elektrokemijske pojave i mnoga druga svojstva o kojima bi se moglo još puno napisati. Detalji se mogu naći npr. u Tehničkoj enciklopediji ili na internetu pod ključnim riječima dispersing, dispersed, colloid, foam, gel, sol, aerosol, emulsion, Tyndall effect, Brownian motion, colloid chemistry itd.
Obavijesti
P.S.
- Ako ne možete odgonetnuti ovdje se radi o simbolu 'korijena'
A) plošno centrirana kocka d = a√3/2
B) volumno centrirana kocka d = a√2/2
Udžbenici i zbirke
Nadam se kako ste mogli pronaći udžbenike kod starijih kolega,
a s kupovinom zbirki ne morate žuriti, možda pronađemo i neko drugo rješenje. 

Tehničke neispravnosti:
U kemijskim jednadžbama oznake zareza trebale bi biti strelice. Kod brojčanih vrijednosti potencije nisu dobro istaknute kao ni brojevi atoma unutar molekula ili formulskih jedinki.

KONZULTACIJE ZA UČENIKE - SVAKE SRIJEDE U 14 h. VRIJEME INFORMACIJA ZA RODITELJE - SRIJEDA, PETI SAT I SVAKI PETAK U 18h. DODATNA NASTAVA IZ KEMIJE SVAKI PETAK U 16 sati (JEDAN TJEDAN MATURANTI, 1. i 2. RAZREDI DRUGI TJEDAN). UČENJE PO PREDMETIMA I DRUŽENJE ZA UČENIKE 2.E RAZREDA - SVAKE SUBOTE U 8 i 30 


